1. はじめに
近年、solvent flattening,histogram matching,averaging等のdensity modificationが、盛ん に蛋白質のX線結晶構造解析に用いられるようになってきた。一般にこれらは、 「解釈の難しい蛋白質の電子密度図に適用することで、電子密度図を改良し、解釈 できるものにする」と言うように理解されているようである。しかし、果たして本 当にそうなのであろうか?もしそれが本当ならば、もう少し構造解析が楽になって もいいのでは無いか?(もちろん、もうすでに十分楽だという気もするが)筆者の 経験からすると、むしろ上に述べたような漠然とした印象というのは、我々蛋白質 結晶学に携わる者の願望に近いような気がする。先日のTARAの講演会でも述べた通 り、私はやはり重原子同型置換体を作る事が最重要であると思う。もちろん私も density modificaionの威力は認めるし、その恩恵にもいくらか預かっている。しかし ながら、どうしても忘れて欲しくないことは、いくらdensity modificationの威力が絶 大であろうとも、density modificationがdensityのmodificationである限り、要するに direct methodでないのならば、初期位相(つまりは重原子同型置換体)の存在が大前 提になっているということである。これは、計算lこ夢中になっているとついつい忘 れがちなことで、計算機の前に座る時間の長い、我々結晶学に携わる者が陥り易い 間違いであるような気がする。
そこで本稿では、実例を交えつつdensity modificationの有効性と限界を述べたいと 思う。そのうえで、density modificationの前提となる初期位相の付け方、要するに重 原子誘導体の作り方に言及する。なお、本稿で言うところのdensity modificationは、 solvent flatteningとhistogam matchingのみで、averagingにはふれません。
2. Solvent flatteningとhistogram matching
Solvent flatteningとhistogam matchingは、現在最も手軽に行えるdensity modificationで ある。CCP4に含まれているプログラムDMを使えば、ほとんど全自動でこれらの処 理を行うことが可能である(マニュアルすら読まなくても流せる!)。では、一体 どのような処理が行われているのだろうか?既にご存じの方も多いとは思うが、簡 単に解説を加える。
Solvent flatteningは、最もポピュラーなdensity modificationである。また、その理論 も理解しやすい。つまり、結晶中の溶媒部分の電子密度はフラットであるはずだか ら、強制的にこれら部分の電子密度を0にしてしまう訳である。このmodifyした電 子密度図を逆フーリエ変換し、MIRの位相情報と組み合わせることで、位相の改 善、つまりは、電子密度を改善していこうという手法である。
これに対し届histogram matchingは何をやっているのか、どうしてこれで位相が改善さ れるのかが、今一つ不明瞭である。この手法は、「蛋白質の電子密度の分布のヒス トグラムをとると、全ての場合にほぼ等しい」という前提に基づいている。そこ で、現在持っている蛋白質部分の電子密度を理想的なヒストグラムにあわせること で、電子密度図を改善していこうという方法である。では、何故これで電子密度図 が改善されるのか?実際に画像処理関係の教科書を見てみると、このヒストグラム をあわせるという操作は、一般的によく行われている手法であることがわかる。し かし、「何故」に関する記述を見つけることは出来なかった。しかし注目すべき は、一旦ヒストグラムを決めてしまえば、maximum entropy method(MEM)で言うとこ ろのエントロピーが規定される点である。これを考えに入れるなら、histogram matching法というのはエントロピーの最大値(に近い値)を先に与え、この値を目指 して電子密度を組み換える方法であるといえる。もちろん、この場合「どのように ヒストグラムを理想の形に一致させるか」という問題点が残っており(理想のヒス トグラムを満足するだけの電子密度分布であれば無限にある)、多分これが最終的 な電子密度の正当性と深く係わっていることは容易に想像できる。しかし、DMのそ れを解析し評価することは筆者の能力を超えているので、本稿ではふれない。
3. Density modificationを用いた分子の外形の決定
では、以上のようなdensity modificationが、どの程度まで有効であるかを実例をあ げつつ述べる。
重原子誘導体がとにかく見つかり、初期位相が付いた段階でのdensity modification は有効なのであろうか?これに対しては、「無理な高望みをしなければ、有効であ る」と言える。つまり、いきなり解釈可能な電子密度図を手に出来るかというと、 これは後に述べるように初期位相の質に大きく依存することになるので、一概には 言えない。但し、初期位相の決定がある程度正しく行われていれば、およその分子 の外形を知る程度のことは可能なのである。
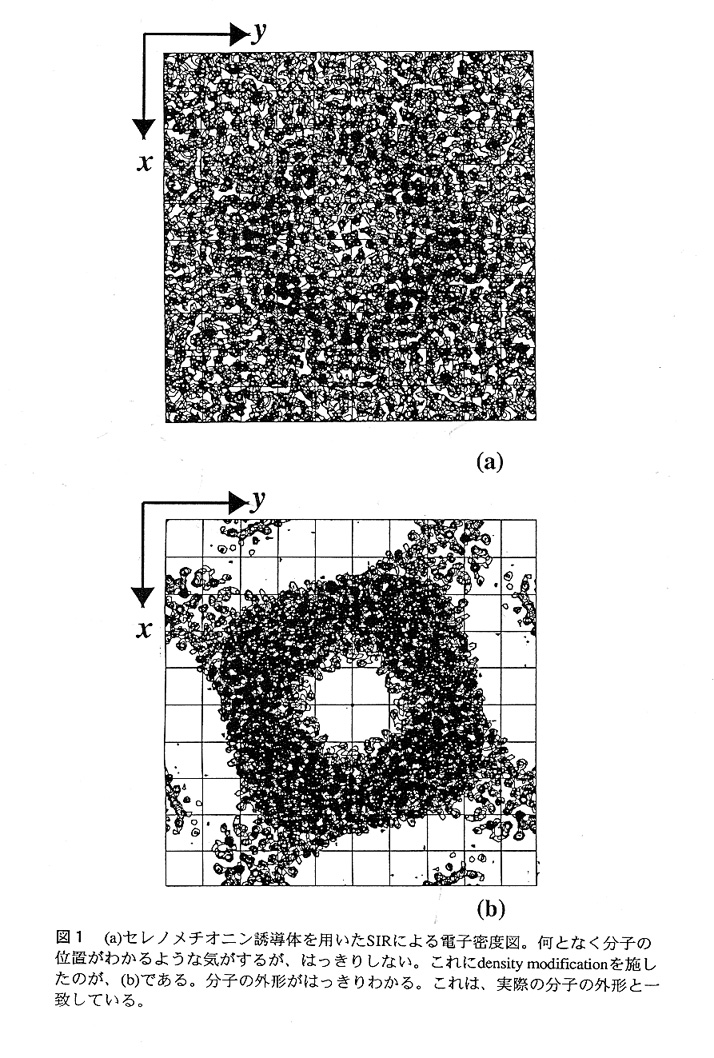
図1(a)に示したのは、BphC酵素の解析における、セレノメチオニン(SeMet〉誘 導体を用いたSIRによる電子密度である(データは、実験室のR-Axisを用いて集めた もので、位相の計算に異常分散の効果は入っていない)。これにDMを適用すること で、図1(b)のような電子密度図を得ることが出来た。この電子密度図と実際の立体 構造を比較すると、分子の外形としては十分な情報を持った電子密度図であること がわかる。
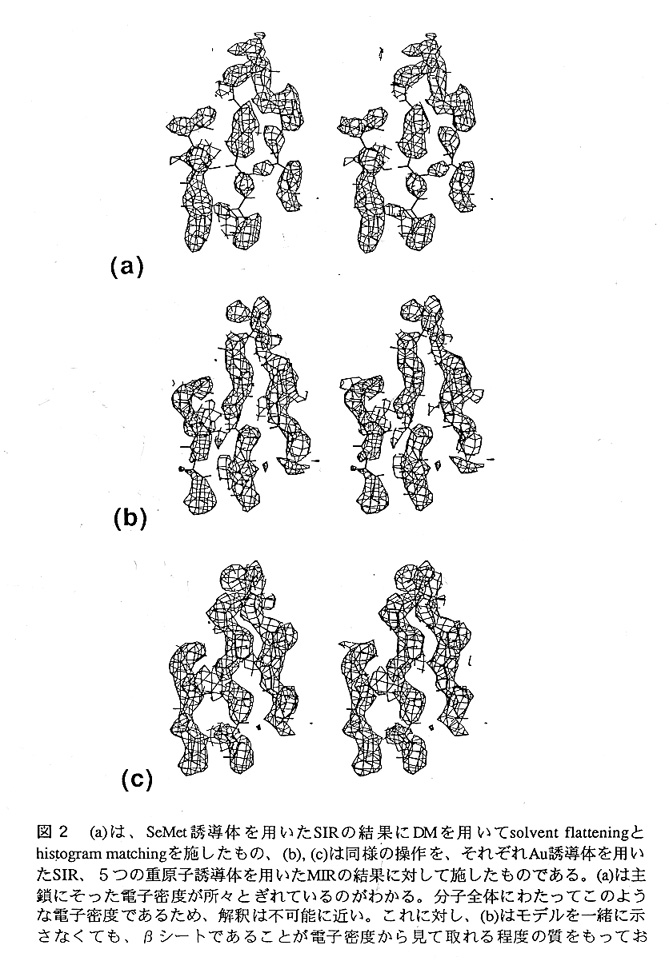
では、この電子密度図は、解釈可能な電子密度図なのであろうか?実際に得られ た電子密度図を細かく検証していくと、この電子密度図を用いて解釈を行いモデル を構築するのは、無理があることがわかる。図2(a)に示したように、部分的には電 子密度図とモデルが一致している様に見える。しかしながら、電子密度図の解釈は 分子全体にわたって行うものであるという事実、不明瞭な部分が増えれば電子密度 図の解釈は指数関数的にやっかいになっていく、という事実を考えれば、図2(a)に 示した電子密度図を使って解釈を行うのはまず不可能である。百歩譲って、経験を 積んだ人なら出来ると言ってみたところで、これでは普通の経験を持つ我々が解け ることにはならず、ダメである。

4. 解釈可能な電子密度図が得られるのか?
では、density modificationを用いて解釈可能な電子密度を得ることは不可能なので あろうか?そんなことは無いのである。これは、多くの論文を見ればわかること で、SIR、SAS等の電子密度図に、density modificationを施すことで立派に構造を決定 している例が多く報告されている。では、何故SeMetの例では、そのような電子密度 図が得られなかったのであろうか?図2(b)に示したのは、金の重原子誘導体による SIRの位相を元にdensity modificationを行った電子密度図である。これを見ると、図2 (a)に示したものとは違い、解釈が出来そうな電子密度であることがわかる。また、 図2(c)に示したMIRの電子密度にdensity modificationを施したものは、非常にきれい な電子密度を与えていることがわかる(もっとも、MIRによって得られた電子密度 図は、そのままで十分解釈が可能な良好なものであった)。
このような差がでてくるのは、何故なのであろうか?一般に言われていることで あるが、density modificationの効果というのは、初期位相によるところが大きい。つ まり、初期位相がよければ、density modificationによって電子密度の改善が望める。 しかし、初期位相が悪ければ、いくらdensity modificationをやったところで正解にた どり着くは難しいと言わざるを得ない。ここで忘れていけないのは、位相情報は、 位相角そのものとfigure of merit(FOM)に分かれて記録されているという点である。 この点は忘れがちであるが、実際にdensity modificationをするときには重要な点であ る。一般にdensity modificationを行うと、FOMの値が改善され(要するに大きくな る)、あたかも位相が良くなったかのごとくの印象を与える。しかしこれは、全く ナンセンスである。重要なのは、そのFOMの増加分に見合う位相角の改善が実 際になされているかどうかが問題であって、FOMの値そのものに位相の改善 を示す積極的な意味は無いと言うことである。要するに、FOMは、フーリエ変換 を行う際に個々の反射にかかるweightであるから、FOMが大きな場合には、それに見 合った正確な位相である必要がある。もし、FOMと位相角の正確さの間に相関が無 ければ、得られる電子密度図はFOMの値の大きさに反して粗末なものになってしま う。これに対し、たとえFOMの値が小さくてもその見積もりが正確であれば、正確 な電子密度図を得ることが可能である。
以上述べたように、figure of merit(FOM)の値の正確さが電子密度図の質に影響を 与えるため、初期位相においてFOMの見積もりの正確さは重要である。最近は、 CCP4のMLPHAREなどの良いプログラムが出回って、これらの値がそれほどおかし いということは無いようである。しかしながら、FOMが如何にdensity modificationの 結果に影響を与えるかを見ておいても悪くないであろう。それを実際に行ったのが 図3である。位相Aは、当研究室で昔使っていたプログラムによりつけた位相、位相 BはCCP4のMLPHAREにより付けた位相である。この両者を此べると、図3の左図か らわかるように、位相角の質は両者でほとんど差がない。ところが、FOMの見積も りを見てみると(図3右図)、位相Aはいささかその見積もりが甘いと言うことがわ かる(原因は、エラーの見積もりの悪さなど色々考えられる)。
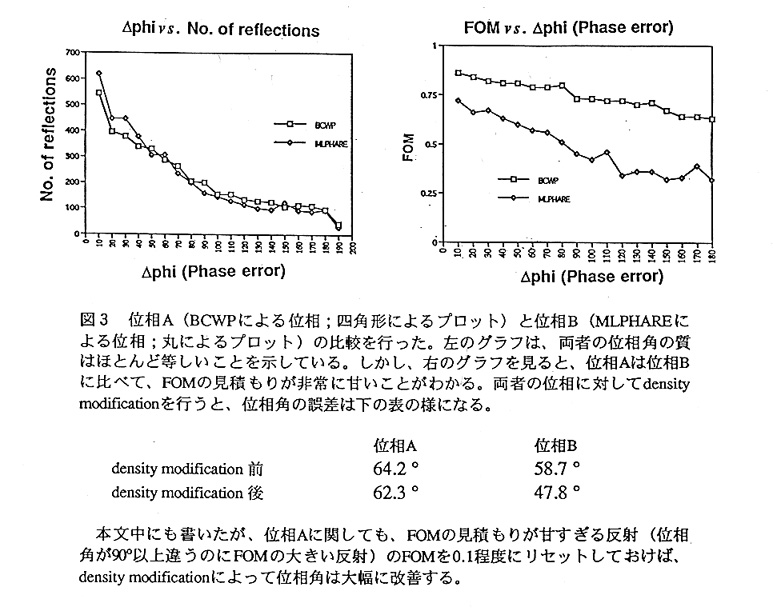
この両者に対して density modificationを行った結果が図3の説明文中に示してある.一目見てわかるよ うに、位相Bの方は位相角の改善がめざましいのに対し、位相Aの方はほとんど位相 角の改善が見られない。これは、位相情報というのは、位相角のみならずFOMにも 含まれるという当然の事実を示すとともに、FOMの見積もりがdensity modificationの 結果に少なからず影響を与えると言うことを示している。実際に、上記の位相Aにお いてFOMの見積もりが大きすぎる反射を選び、これを全て0.1にリセットすれば、 density modificationの結果、位相が大幅に改善されることを確かめることが出来た。 では、FOMの値はdensity modificationによってどのように変化するのであろうか? また、FOMの見積もりは適正に行われるのであろうか?これらの事を調べるため に、図4に示すような解析を行った。これらのグラフを見ると、セレノメチオニン のSlRで得た位相にDMを施したものは(図4(a)を参照)、正しくない位相角の一群 に対し(FOM(calc)がほとんど0の反射に対し)、プログラムはほとんど1に近い FOMを付けていることがわかる。これに対し、このようなFOMの見積もりが大きく 違う反射は、金の誘導体のSIR、MIRと初期位相が良くなるにつれて少なくなって いっていることがわかる。
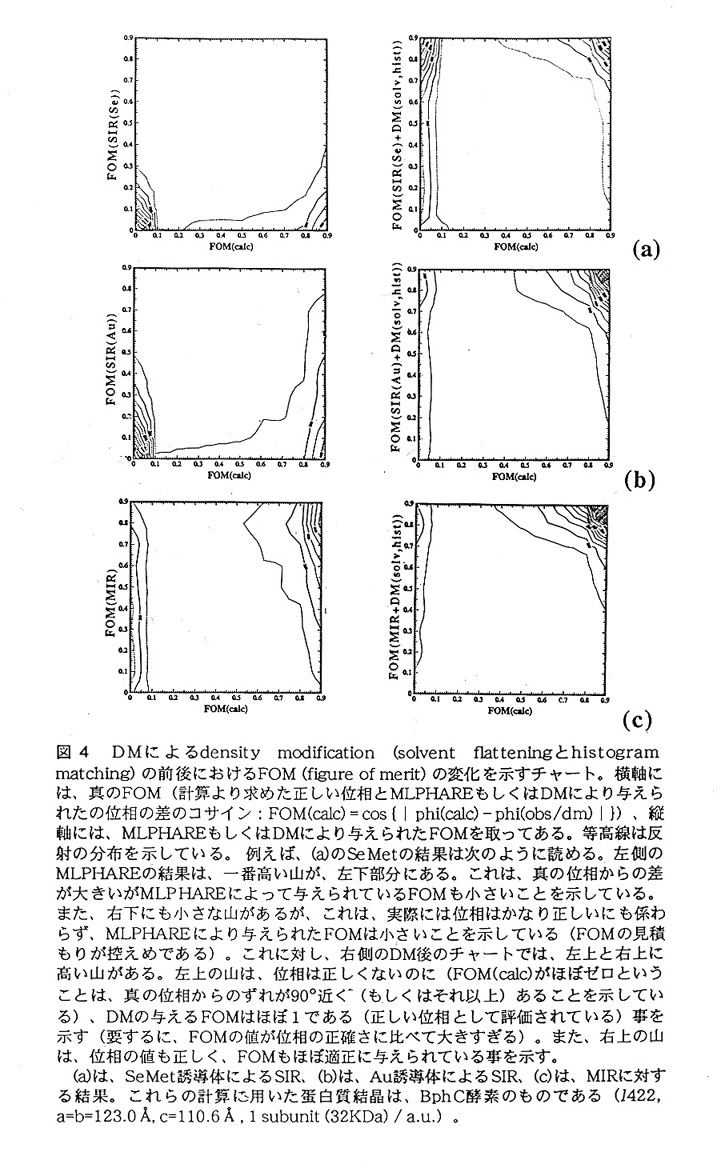
これらの事実から、以下のような事がいえる。まず第一に、初期位相が悪ければ density modificationによる電子密度の改善(ここで言うのは、解釈が可能な程度まで の電子密度の改善)は難しい。第二として、density modificationを施すことによっ て、位相角が改善してもしなくても、FOMの値は大きくなる傾向がある。そのた め、一度間違えた方向に行ってしまった位相角が(FOMの見積もりが違っている初 期位相の例を考えればわかるように)、正しい方向に戻ってくることはまずあり得 ない。つまり、現状では、潜在的に悪い初期位相を用いてる限り、いくらdensity modificationをやったところで正しい位相角及び適正なFOMの値を得られるとは思 えない。逆に言えば、現状では、density modificationには"正しい"初期位相が必要 であると言うことになる(これは、必ずしも初期位相のFOMが大きいと言うことを 意味しない。むしろ、各重原子誘導体のRcullis等の値をしっかりと見ていた方が良い であろう)。
今まで述べて来たようにFOM等の統計値は役に立たないのであれば、何を基準に 位相の良否を判断すべきなのであろうか?特にdensity modifncationを施した後では、 得られた位相の良否に係わらずFOMは総じて大きくなっているものである。このよ うな場合(というか一般的に)位相の良否は、電子密度図を見て判断する以外に方 法は無いのである。具体的には、電子密度中に、αヘリックスやβシート等の2次 構造が見えるかどうか、というのが一般的な判断基準である。もしこれらの2次構 造が電子密度中に見えるのならば、その電子密度はもっともらしいし、位相も信頼 できるものである。逆に何の2次構造も見い出せず、何やら意味不明のペプチド鎖 の様なものが「うねうね」と見えるだけならば、その電子密度は信頼できるもので は無い、と判断せざるを得ず、位相もとうてい信頼できるものではない。何やら、 漠然とした印象を受けるかも知れないが、信頼できる客観的な統計値が無い以上、 これ以外に基準は無いであろう。
5.よりよい初期位相を得るために
以上、density modificationを行う際の初期位相の重要性について述べてきた。で は、どのようにしてよりよい初期位相をみつければ良いのだろうか?これはもう実 験以外に方法は無い。重原子同型置換体の探索を徹底的に行う以外、これといった 方法は無いのではないだろうか?もちろん、場合によっては(タンパク質工学的手 法等を応用して)作為的に重原子サイトを作ることも可能な場合があるのかもしれ ないが、いつでも可能な手法では無い。
当グループでは、かなりしつこく重原子サーチを行っている。この際に最も頻繁 に起こる問題は、重原子溶液に結晶をソーキングした時に結晶が壊れてしまうこと である。このようなときは、一回であきらめず数回試してみることも必要である。 たまに壊れない結晶が得られることもあるし、良く調べてみると重原子溶液のpHが 違っていることもある。特にpHの違いは、致命的であることが多い。結晶が壊れる 原因としては、もちろん重原子がタンパク質に結合して結晶格子を破壊している場 合もあるが、pHの違いによって結晶が壊れてしまうことも多いことを考えに入れて おく必要がある。一般に重原子溶液は、それ程大量に作るわけにも行かないので (通常1ml程度のものであろう)そのpHを正確に測るには、微小電極を使用する必要 がある。重原子同型置換体のスクリーニングをする前に、この微小電極がきちんと 機能するかどうかを確かめておくことも大切である。電極の反応が鈍いようなら、 新しいものに取り替えて、しっかりと校正をしてから使用すべきである。実際に、 このような些細なことで、仕事がうまく行かないこともあるのである。もちろん、 これらのことは特別なことではないので、多くの研究室で実際に行われていること だろう。しかし、最終的に数百の条件を調べることはたしかに面倒臭く、ついつい これらのことは、「わかっちゃいるけど・・・」となりがちである上に、density modificationに過度の期待を抱きすぎると、重原子サーチの手も鈍くなってくるもの である。先日の討論でも、結局のところ、density modificationを成功させるには、" 良い"重原子同型置換体が必要であると言うことで意見の一致を見たと思う。更に 一度でもMIRによる解析を行ったことのある人なら知っていることであるが、多く の場合MIRによる解析においても位相決定に効いているのは1つもしくは2つの" 良い"重原子同型置換体なのである。もちろん、場合によっては使用できるサンプ ルの量に限度があったりと、必ずしも十分な実験が出来るわけではないのは事実で あろう。そのときは、density modificationを効果的に使用することが必要であること は筆者も承知している。それでもあえてこのようなことをぐだぐだと書くのは、 MIRにしろSIR(SAS)+density modificationによる解析にしろ、元となるのは"良い"重 原子同型置換体であることはいくら強調してもしすぎることは無いと考えているか らである。MlRによる解析でも、たいていの場合最終的にはdensity modificationによ る"整形"をやるのだから、MIRによる解析を行うか、SIR(もしくはSAS)に加えて density modificationを用いた解析を行うかなどと言うことは、"良い"重原子同型置 換体を手にしてから考えればいいような気がするのである。