1. はじめに
Src-ホモロジー3(SH3)ドメインは、srcファミリィのプロテインキナーゼに保存される50-75残基程度のドメインとして同定され、細胞内シグナル伝達に関与する蛋白分子の多くにその存在が認められている。SH3ドメインは、細胞内シグナル伝達において、標的蛋白分子のプロリンリッチモチーフを結合し蛋白-蛋白複合体形成行う蛋白モジュール(アダプター)であると考えられている。その構造生物学的研究も活発に行われ、現在ではドメインの立体構造やプロリンリッチモチーフを含むオリゴペプチドの結合様式について多くの知見が得られている。
著者は、SH3ドメインの構造生物学的研究が報告され始めた1993年から1996年の間、英国Ludwig Institute for Cancer Reasearch(M.D.Waterfield教授)に在籍し細胞内シグナル伝達に関与する蛋白のドメインについてモデリングを中心とした研究を行ってきた。本稿では、著者が Ludwig Institute for Cancer Reasearch 在籍中に行った食細胞NADPHオキシダーゼ活性化因子p67phoxのC-端SH3ドメインのリガンドの結合様式に関する研究1)を紹介する。
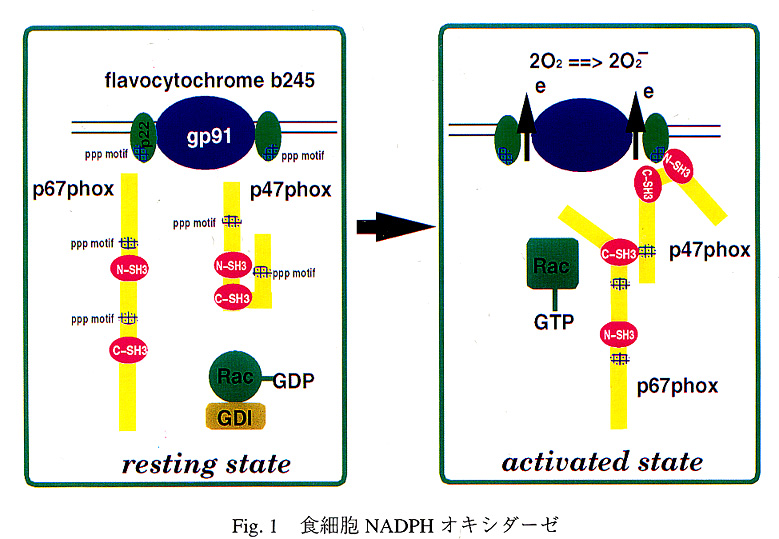
2. 食細胞NADPHオキシダーゼ複合体(Fig.1) 食細胞NADPHオキシダーゼ複合体は、細胞質に存在する3つの因子、p47phox,p67phox及びRac1/2と酵素本体である膜貫通性のフラボシトクロームb558からなり、分子状酸素からスーパーオキサイドを生成する2,3。その活性化は、食細胞に対する刺激によるp47phoxとp67phoxが細胞膜へ移行とそれらのフラボシトクロームb558及びRac1/2との複合体の形成によって引き起こされる。p47phoxとp67phoxにはそれぞれ2つのSH3ドメインが存在し、それらは食細胞NADPHオキシダーゼ複合体の活性化に必要であることが知られている4。 p47phoxのSH3ドメインはresting stateでは、自分自身のC-末端領域近傍の proline-richモチーフと結合しマスクされた状態であり、活性化に伴い露出し、p22phoxの細胞質側に露出したproline-richモチーフに結合すると考えられている5,6。

P.Finan らのグループは、HL60細胞のlysate と p47phox,p67phoxを含む8種類のSH3ドメインを固定化したアフィニティマトリックスを用いて、p47phoxがp67phox C-SH3 ドメインに特異的に結合するが、他のSH3ドメインには結合しないこと、さらにp47phoxのC-末端領域近傍のproline-richモチーフがこの結合に重要であり、同領域に相当する合成ペプチドQPAVPPRPがこの結合を阻害することを見いだしていた7。
著者らは、これらの知見に基づき、p67phox C-SH3 ドメインとペプチドQPAVPPRPの複合体のモデリングに着手した。
3. p67ph1oxC-SH3ドメインとp47phox 由来ペプチド複合体のモデリング 著者らがモデリングに着手した時点では、9個のSH3ドメインの構造(リガンド複合体の構造2個を含む)が報告されていた8-16 。
すべてのSH3ドメインにおいて、その toppology は、2つのβシートからなるコンパクトな barrel-like fold として特徴づけられ、非常によく保存されていた(Fig.2)。リガンド結合部位は、よく保存された芳香族残基からなる3つの疎水性ポケットと2つのループ(RT-loop,n-src-loop)により構成され、PxxPモチーフを含む7-10残基程度のぺプチド性リガンドがpolyproline type-Ⅱ(PPⅡ)ヘリックス構造をとってこの部位に結合していることが明らかとなっていた(Fig.3)。
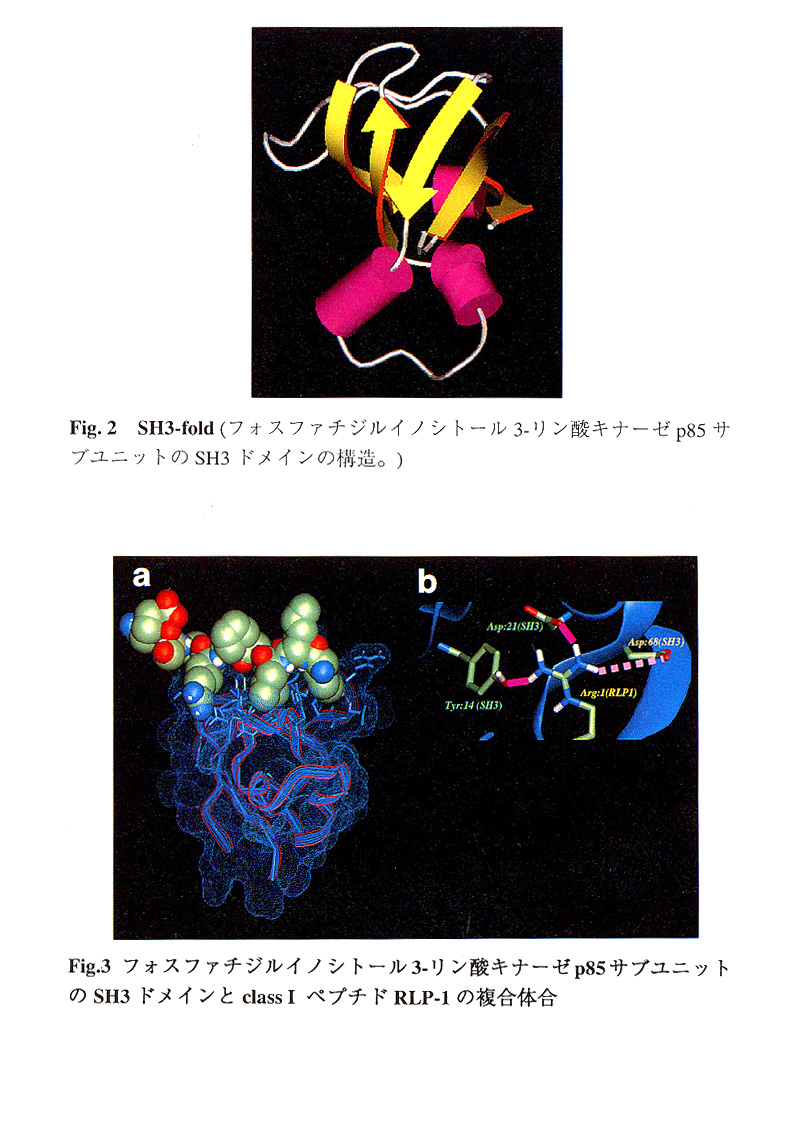
また、ペプチドライブラリィを用いた実験により、PxxPモチーフを含むSH3ドメインのリガンドはclass Ⅰ,Ⅱの2つのタイプに分類されていた。Class ⅠリガンドのSH3ドメインに対する結合様式は、フォスファチジルイノシトール3キナーゼp85サブユニット(PI3Kp85)のSH3ドメインとの複合体の構造を解析することにより明らかとなり、N-末端のArgは、RT-loopのAsp21と静電的に相互作用していることが示された16(Fig.4)。Class Ⅱのペプチドはそのアミノ酸配列(Class ⅠではPxxPモチーフのN-末端、Class ⅡではPxxPモチーフのC-末端にArg残基が位置する。)やPPⅡへリックス構造の擬対称性から、Class Ⅰと逆向きの(minus orientation)結合様式の可能性が指摘されていた16。
著者らは、これらの知見をふまえplus orientation及びminus orientationで結合したp67phox C-SH3ドメインと合成ペプチドQPAVPPRPの複合体モデルを作成した。p67phox C-SH3ドメインのテンプレートには、c-abl SH3ドメインを用いた(Fig.5)。
前述の既に構造解析されていた他のSH3ドメイン-proline-richペプチド複合体では、SH3ドメインとproline-richペプチドのジオメトリーの相補性が重要であることが明らかとなっている。著者らが得たいずれのモデル構造に於いてもペプチドのジオメトリーはSH3ドメインにフットし、SH3ドメインのリガンド結合サイトのよく保存されている3つの疎水性領域で好ましい疎水相互作用をすることが期待された。ペプチドリガンドQPAVPPRPのArg残基は、プラスオリエンテーションの複合体ではGlu53静電相互作用する可能性が、マイナスオリエンテーションではAsp16とGlu15と水素結合することが予測された(Fig.6)。
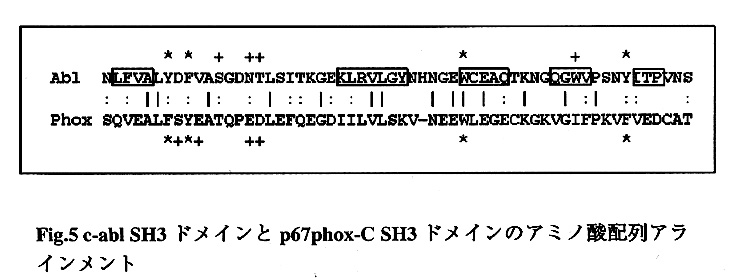
2つのドメイン問で保存されている残基(|)と性質が類似した残基(:)を示した。リガンド結合ポケットで保存されている疎水性残基は*で、直接リガンド結合に関わっている残基は+で示した。c-abl SH3ドメイン(x-線結晶構造)のβ-ストランドを枠で示した。
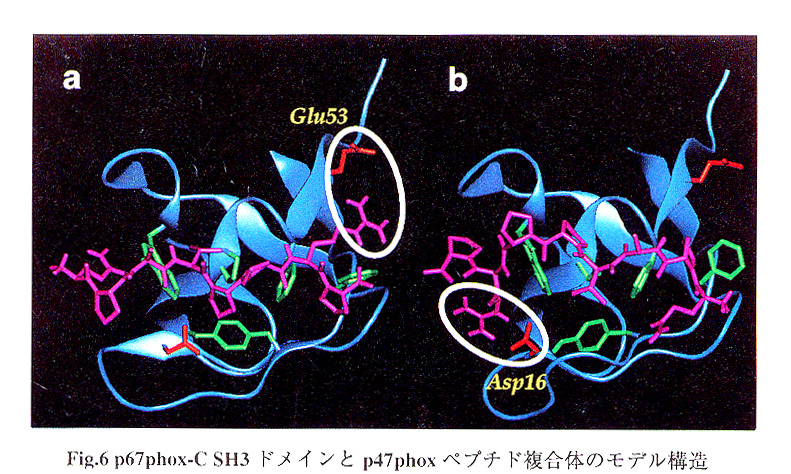
plus-orientation(a) 及び minus-orientation(b)で結合した複合体のモデル構造を示した。SH3ドメインのβ-シート部分はリボン表示した。p47phoxペプチド(紫)、SH3のリガンド結合ポケットを構成する疎水性残基(緑)、それぞれのorientationでペプチドのArg残基と静電相互作用する可能性がある残基(赤色)をスティックモデルで示した。
4. 部位特異的変異を導入した変異体を用いた結合能の評価
先の2つのモデルに基づいて、それぞれのオリエンテーションに劇的に影響を及ぼすと考えられる部位特異的変異を導入したp67phox C-SH3ドメイン変異体を調製しその食細胞の lysate 中の p47phox に対する結合能を評価した。
plus-orienhltonの結合能に影響を与える可能性がある変異体
Glu53は、ペプチドリガンドQPAVPPRPがplus-orientatonで結合した場合、ペプチドのArg残基と静電相互作用する可能性が予想された残基である。p67phox C-SH3ドメインのGlu53をAsn,Ala,Glnに置換した変異体を調製した。試みた3つの変異体いずれも、食細胞のlysateのp47phoxに対する結合能には、変化は見られなかった。
ペプチドRLP-1はpolyproline type-Ⅱ(PPⅡ)ヘリックス構造をとってこの部位に結合している(a)。N-末端のArgは、RT-loopのAsp21,Asp68と静電的に相互作用している16(b)。
minus-orientation の結合能に影響を与える可能性がある変異体
Asp16は、ペプチドリガンドQPAVPPRPがminus-orientatonで結合した場合、ペプチドのArg残基と水素結合することが期待される残基である。p67phox C-SH3ドメインのAsp16をAlaまたはSerに置換した。これらの変異体では、p47phoxに対する結合能が明らかに減弱した。Asp16をGluに置換した場合も結合能の低下が認められた。
これらの実験結果は、p67phox C-SH3ドメインとp47phoxの結合はminus-orientatonであることを強く示唆するものであった。
5. src SH3-RLP1(AFAPPLPRR)複合体構造との比較(Fig.7)
著者らの研究中に、複数のグループからSH3ドメインとprohne-richペプチドがminus-orientationで結合した構造が報告された17-19。 src SH3ドメインとペプチドRLP1の複合体構造もその一つである17。NMRにより構造解析されたこの複合体とp67phox C-SH3ドメインとQPAVPPRPのマイナスオリエンテーション複合体モデルの構造の比較を行った(Fig.7)。
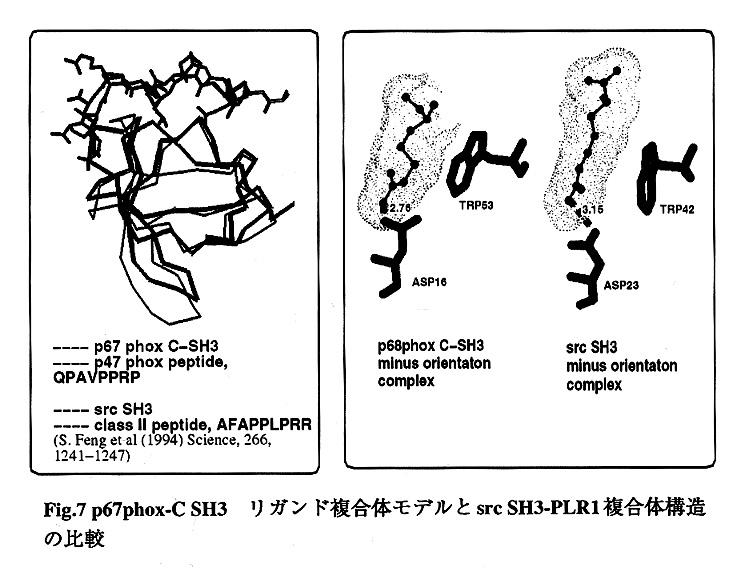
2つのSH3ドメインの重ね合わせの結果から全体的なトポロジーが非常によく保存されていることが示された。いずれの構造においてもリガンドペプチドのArg残基はSH3ドメインのRT-loop上のAsp残基と水素結合しており、SH3のTrp残基に対し同様なパッキングを示していることが明らかとなった。このような構造の類似性から著者らのモデルがminus-orientationで結合したSH3-proline-richペプチド複合体の特徴を備えていることが示された。
SH3ドメインがproline-richモチーフを含むリガンドをマイナスオリテンテーションで結合することは、いくつかのSH3ドメインについて報告されているがこれらはすべてSH3ドメインとペプチドの相互作用としての検討である。ここに示したp67phox C-SH3ドメインとp47phoxの結合は、生理学的に意味のある全長の蛋白分子に存在するproline-richモチーフもマイナスオリエンテーションで結合しうることを実験的に初めて示した例である。
6. おわりに
NADPHオキシダーゼは、食細胞による殺菌作用に必須な酵素であるが、その異常な活性化はスーパーオキシドの過剰産生を引き起こしリュウマチなどの慢性炎症性疾患の主たる原因であると考えられている20。近年、NADPHオキシダーゼの活性の制御に関する研究が精力的に行われ、活性化したこの酵素複合体におけるSH3ドメインの重要性が明らかとなってきた4-6。本稿にも述べたようにp67phox C-SH3ドメインとp47phoxの結合は他のSH3ドメインとproline-richモチーフの結合と異なり非常に特異的であり、この相互作用は、酵素活性を制御するリガンドの作用点としても興味が持たれる。Schreiberらは、src SH3ドメインに対する非ペプチド性リガンドを見いだすことを目的として構造生物学とコンビナトリアルケミストリーを組み合わせた方法を報告している21。SH3ドメインを作用点としてNADPHオキシダーゼ複合体の酵素活性を制御するリガンドが得るアプローチの一つとして興味深い。
この研究は、Yamanouchi Research Institute の P.Finann博士、S.Kellie博士、Ludwig Institute for Cancer ResearchのM.Zvelebil博士、M.D.Waterfiled教授との共同で行われたものである。また、彼らとの共同研究の機会を与えていただいた山之内製薬株式会社に感謝の意を表したい。
文献